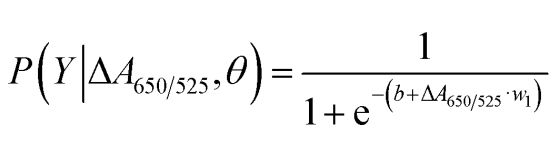La detección precoz del cáncer mediante biopsia líquida es una nueva línea de investigación propuesta por el Instituto Nacional del Cáncer de Estados Unidos en los últimos años, con el objetivo de detectar el cáncer en sus etapas iniciales e incluso lesiones precancerosas. Se ha utilizado ampliamente como un biomarcador novedoso para el diagnóstico precoz de diversas neoplasias malignas, como el cáncer de pulmón, los tumores gastrointestinales, los gliomas y los tumores ginecológicos.
La aparición de plataformas para identificar biomarcadores del panorama de metilación (Methylscape) tiene el potencial de mejorar significativamente la detección temprana del cáncer existente, colocando a los pacientes en la etapa tratable más temprana.
Recientemente, investigadores han desarrollado una plataforma de detección simple y directa para el análisis del perfil de metilación, basada en nanopartículas de oro recubiertas con cisteamina (Cyst/AuNPs) y un biosensor para smartphone. Esta plataforma permite la detección temprana y rápida de una amplia gama de tumores. La detección precoz de la leucemia puede realizarse en 15 minutos tras la extracción de ADN de una muestra de sangre, con una precisión del 90 %. El título del artículo es «Detección rápida de ADN cancerígeno en sangre humana mediante nanopartículas de oro recubiertas con cisteamina y un smartphone con aprendizaje automático».
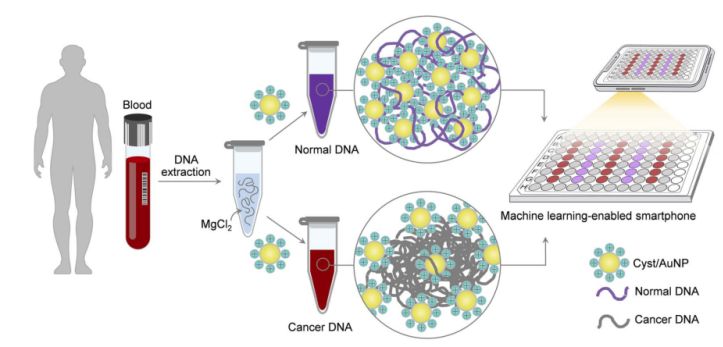
Figura 1. Se puede lograr una plataforma de detección simple y rápida para el cribado del cáncer mediante componentes de quistes/nanopartículas de oro en dos sencillos pasos.
Esto se muestra en la Figura 1. Primero, se utilizó una solución acuosa para disolver los fragmentos de ADN. Luego se añadieron los quistes/nanopartículas de oro (Cyst/AuNPs) a la solución resultante. El ADN normal y el maligno presentan diferentes propiedades de metilación, lo que da lugar a fragmentos de ADN con distintos patrones de autoensamblaje. El ADN normal se agrega de forma laxa y, finalmente, agrega los Cyst/AuNPs, lo que provoca un desplazamiento al rojo en estos últimos, de modo que se puede observar un cambio de color de rojo a púrpura a simple vista. En contraste, el perfil de metilación único del ADN canceroso conduce a la formación de cúmulos más grandes de fragmentos de ADN.
Se tomaron imágenes de placas de 96 pocillos con la cámara de un teléfono inteligente. El ADN canceroso se midió con un teléfono inteligente equipado con aprendizaje automático, en comparación con métodos basados en espectroscopia.
Detección del cáncer en muestras de sangre reales
Para ampliar la utilidad de la plataforma de detección, los investigadores aplicaron un sensor que logró distinguir con éxito entre ADN normal y canceroso en muestras de sangre reales. Los patrones de metilación en los sitios CpG regulan epigenéticamente la expresión génica. En casi todos los tipos de cáncer, se ha observado que los cambios en la metilación del ADN y, por lo tanto, en la expresión de los genes que promueven la tumorigénesis, se alternan.
Como modelo para otros cánceres asociados con la metilación del ADN, los investigadores utilizaron muestras de sangre de pacientes con leucemia y controles sanos para investigar la eficacia del perfil de metilación en la diferenciación de cánceres leucémicos. Este biomarcador del perfil de metilación no solo supera a los métodos de detección rápida de leucemia existentes, sino que también demuestra la viabilidad de extenderlo a la detección temprana de una amplia gama de cánceres mediante este ensayo sencillo y directo.
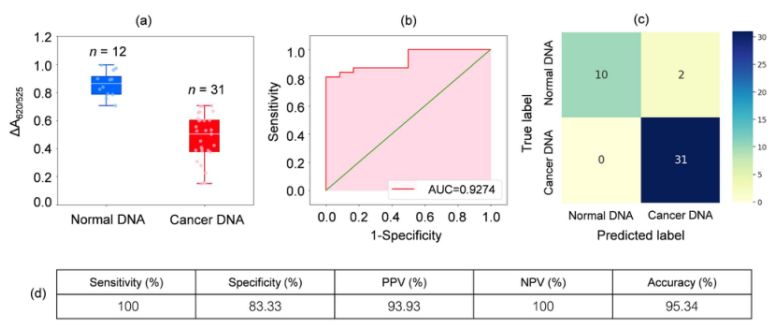
Se analizó el ADN de muestras de sangre de 31 pacientes con leucemia y 12 individuos sanos. Como se muestra en el diagrama de caja de la Figura 2a, la absorbancia relativa de las muestras de cáncer (ΔA650/525) fue menor que la del ADN de las muestras normales. Esto se debió principalmente a la mayor hidrofobicidad que provocó una agregación densa del ADN canceroso, lo que impidió la agregación de Cyst/AuNPs. Como resultado, estas nanopartículas se dispersaron completamente en las capas externas de los agregados cancerosos, lo que resultó en una dispersión diferente de Cyst/AuNPs adsorbidos en los agregados de ADN normal y canceroso. Luego se generaron curvas ROC variando el umbral desde un valor mínimo de ΔA650/525 hasta un valor máximo.
Figura 2.(a) Valores de absorbancia relativa de soluciones de quistes/AuNPs que muestran la presencia de ADN normal (azul) y canceroso (rojo) en condiciones optimizadas.
(DA650/525) de diagramas de caja; (b) Análisis ROC y evaluación de pruebas diagnósticas. (c) Matriz de confusión para el diagnóstico de pacientes normales y con cáncer. (d) Sensibilidad, especificidad, valor predictivo positivo (VPP), valor predictivo negativo (VPN) y precisión del método desarrollado.
Como se muestra en la Figura 2b, el área bajo la curva ROC (AUC = 0,9274) obtenida para el sensor desarrollado mostró alta sensibilidad y especificidad. Como se puede ver en el diagrama de caja, el punto más bajo que representa el grupo de ADN normal no está bien separado del punto más alto que representa el grupo de ADN canceroso; por lo tanto, se utilizó regresión logística para diferenciar entre los grupos normal y canceroso. Dado un conjunto de variables independientes, estima la probabilidad de que ocurra un evento, como un grupo canceroso o normal. La variable dependiente varía entre 0 y 1. El resultado es, por lo tanto, una probabilidad. Determinamos la probabilidad de identificación de cáncer (P) basada en ΔA650/525 de la siguiente manera.
donde b=5,3533,w1=-6,965. Para la clasificación de muestras, una probabilidad menor a 0,5 indica una muestra normal, mientras que una probabilidad de 0,5 o mayor indica una muestra cancerosa. La figura 2c muestra la matriz de confusión generada a partir de la validación cruzada de exclusión de variables, que se utilizó para validar la estabilidad del método de clasificación. La figura 2d resume la evaluación de la prueba diagnóstica del método, incluyendo la sensibilidad, la especificidad, el valor predictivo positivo (VPP) y el valor predictivo negativo (VPN).
Biosensores basados en teléfonos inteligentes
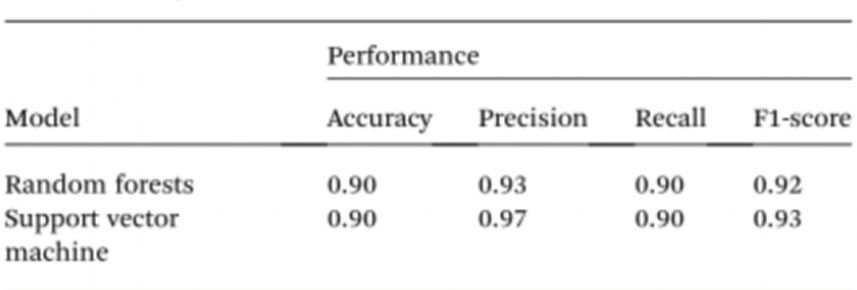
Para simplificar aún más las pruebas de muestras sin el uso de espectrofotómetros, los investigadores emplearon inteligencia artificial (IA) para interpretar el color de la solución y distinguir entre individuos sanos y cancerosos. Para ello, se utilizó visión artificial para convertir el color de la solución de quiste/AuNPs en ADN normal (púrpura) o ADN canceroso (rojo) a partir de imágenes de placas de 96 pocillos tomadas con la cámara de un teléfono móvil. La inteligencia artificial puede reducir costes y mejorar la accesibilidad en la interpretación del color de las soluciones de nanopartículas, sin necesidad de accesorios ópticos para smartphones. Finalmente, se entrenaron dos modelos de aprendizaje automático, Random Forest (RF) y Support Vector Machine (SVM), para construir los modelos. Ambos modelos, RF y SVM, clasificaron correctamente las muestras como positivas y negativas con una precisión del 90,0 %. Esto sugiere que el uso de inteligencia artificial en la biodetección mediante teléfonos móviles es totalmente viable.
Figura 3. (a) Clase objetivo de la solución registrada durante la preparación de la muestra para la etapa de adquisición de imágenes. (b) Imagen de ejemplo tomada durante la etapa de adquisición de imágenes. (c) Intensidad de color de la solución de quiste/AuNPs en cada pocillo de la placa de 96 pocillos extraída de la imagen (b).
Utilizando Cyst/AuNPs, los investigadores han desarrollado con éxito una plataforma de detección sencilla para el análisis del patrón de metilación y un sensor capaz de distinguir el ADN normal del ADN canceroso en muestras de sangre reales para la detección de la leucemia. El sensor desarrollado demostró que el ADN extraído de muestras de sangre reales podía detectar de forma rápida y rentable pequeñas cantidades de ADN canceroso (3 nM) en pacientes con leucemia en 15 minutos, con una precisión del 95,3 %. Para simplificar aún más el análisis de muestras, eliminando la necesidad de un espectrofotómetro, se utilizó el aprendizaje automático para interpretar el color de la solución y diferenciar entre individuos sanos y cancerosos mediante una fotografía tomada con un teléfono móvil, logrando también una precisión del 90,0 %.
Referencia: DOI: 10.1039/d2ra05725e
Fecha de publicación: 18 de febrero de 2023
 中文网站
中文网站