Nat Med | Un enfoque multiómico para mapear el panorama integrado tumoral, inmunitario y microbiano del cáncer colorrectal revela la interacción del microbioma con el sistema inmunitario.
Aunque en los últimos años se han estudiado exhaustivamente los biomarcadores del cáncer de colon primario, las guías clínicas actuales se basan únicamente en la estadificación tumor-ganglio linfático-metástasis y la detección de defectos en la reparación de errores de emparejamiento del ADN (MMR) o inestabilidad de microsatélites (MSI) (además de las pruebas patológicas estándar) para determinar las recomendaciones de tratamiento. Los investigadores han observado una falta de asociación entre las respuestas inmunitarias basadas en la expresión génica, los perfiles microbianos y el estroma tumoral en la cohorte de cáncer colorrectal del Atlas del Genoma del Cáncer (TCGA) y la supervivencia del paciente.
A medida que ha avanzado la investigación, se ha observado que las características cuantitativas del cáncer colorrectal primario, incluyendo la naturaleza celular, inmunitaria, estromal o microbiana del cáncer, se correlacionan significativamente con los resultados clínicos, pero aún se desconoce en gran medida cómo sus interacciones afectan los resultados de los pacientes.
Para analizar la relación entre la complejidad fenotípica y el pronóstico, un equipo de investigadores del Instituto Sidra de Investigación Médica en Qatar desarrolló y validó recientemente una puntuación integrada (mICRoScore) que identifica a un grupo de pacientes con buenas tasas de supervivencia mediante la combinación de características del microbioma y constantes de rechazo inmunitario (ICR). El equipo realizó un análisis genómico exhaustivo de muestras congeladas de 348 pacientes con cáncer colorrectal primario, incluyendo la secuenciación de ARN de tumores y tejido colorrectal sano correspondiente, la secuenciación del exoma completo, la secuenciación profunda del receptor de células T y del gen 16S rRNA bacteriano, complementada con la secuenciación del genoma tumoral completo para caracterizar aún más el microbioma. El estudio se publicó en Nature Medicine con el título «Un atlas integrado de tumores, inmunidad y microbioma del cáncer de colon».

Artículo publicado en Nature Medicine.
Descripción general de AC-ICAM
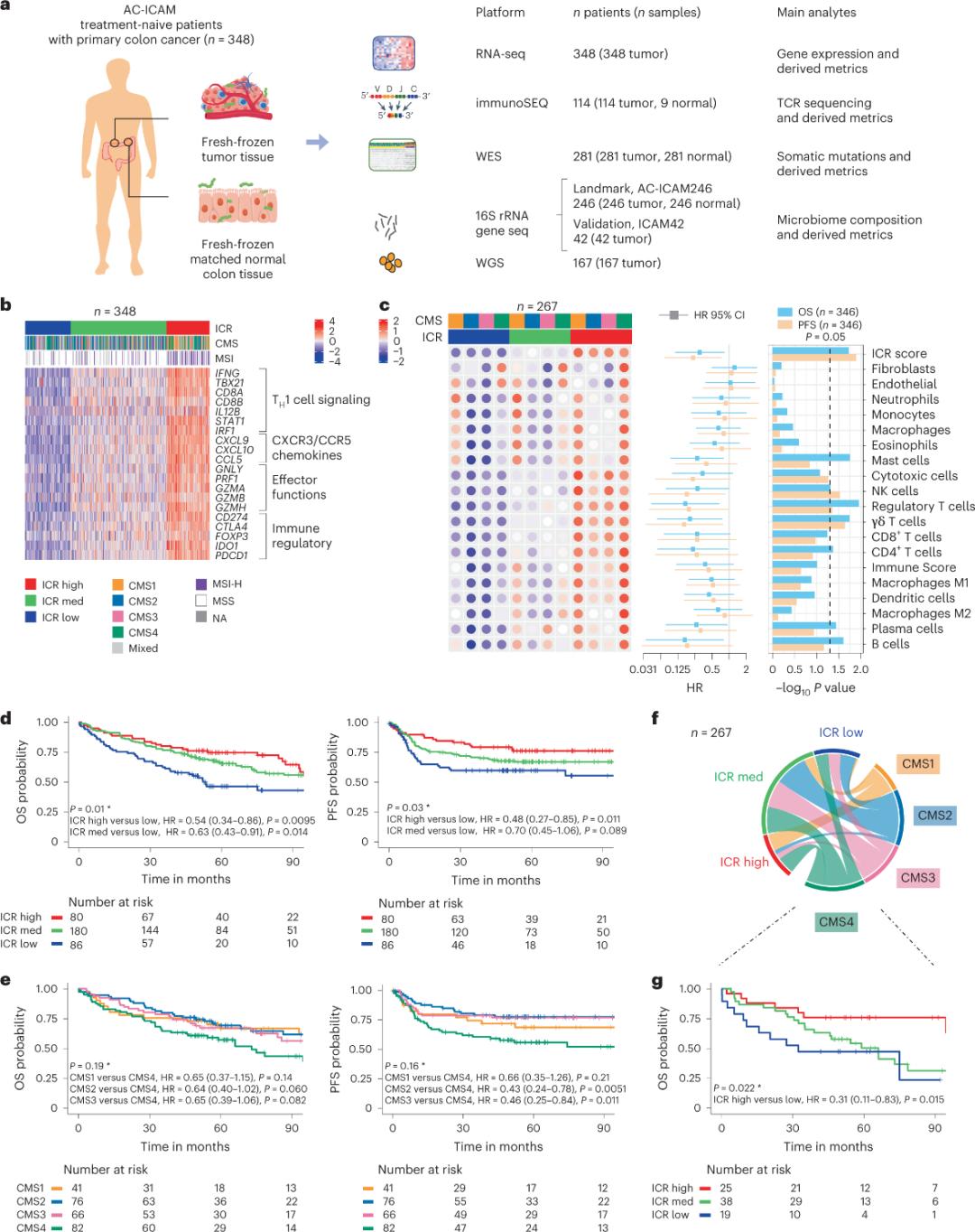
Los investigadores utilizaron una plataforma genómica ortogonal para analizar muestras de tumores congelados y tejido colónico sano adyacente (pares tumor-normal) de pacientes con diagnóstico histológico de cáncer de colon sin tratamiento sistémico. Tras la secuenciación del exoma completo (WES), el control de calidad de los datos de secuenciación de ARN (RNA-seq) y la selección de criterios de inclusión, se retuvieron los datos genómicos de 348 pacientes para su posterior análisis, con un seguimiento medio de 4,6 años. El equipo de investigación denominó a este recurso Sidra-LUMC AC-ICAM: un mapa y guía de las interacciones entre el sistema inmunitario, el cáncer y el microbioma (Figura 1).
Clasificación molecular mediante ICR
Mediante la identificación de un conjunto modular de marcadores genéticos inmunitarios para la inmunovigilancia continua del cáncer, denominado constante inmunitaria de rechazo (ICR, por sus siglas en inglés), el equipo de investigación optimizó la ICR condensándola en un panel de 20 genes que abarca diferentes tipos de cáncer, como el melanoma, el cáncer de vejiga y el cáncer de mama. La ICR también se ha asociado con la respuesta a la inmunoterapia en diversos tipos de cáncer, incluido el cáncer de mama.
Primero, los investigadores validaron la firma ICR de la cohorte AC-ICAM, utilizando un enfoque de coclasificación basado en genes ICR para clasificar la cohorte en tres grupos/subtipos inmunitarios: ICR alto (tumores calientes), ICR medio e ICR bajo (tumores fríos) (Figura 1b). Los investigadores caracterizaron la propensión inmunitaria asociada con los subtipos moleculares de consenso (CMS), una clasificación basada en el transcriptoma del cáncer de colon. Las categorías CMS incluyeron CMS1/inmunitario, CMS2/canónico, CMS3/metabólico y CMS4/mesenquimal. El análisis mostró que las puntuaciones ICR estaban correlacionadas negativamente con ciertas vías de células cancerosas en todos los subtipos CMS, y se observaron correlaciones positivas con vías inmunosupresoras y relacionadas con el estroma solo en los tumores CMS4.
En todos los CMS, la abundancia de células asesinas naturales (NK) y subconjuntos de células T fue mayor en los subtipos inmunitarios con ICR alto, con mayor variabilidad en otros subconjuntos de leucocitos (Figura 1c). Los subtipos inmunitarios de ICR tuvieron diferentes SG y SLP, con un aumento progresivo de ICR de bajo a alto (Figura 1d), lo que valida el papel pronóstico de ICR en el cáncer colorrectal.
Figura 1. Diseño del estudio AC-ICAM, firma genética relacionada con el sistema inmunitario, subtipos inmunitarios y moleculares y supervivencia.
La ICR captura células T amplificadas clonalmente y enriquecidas con células tumorales.
Solo una minoría de células T que infiltran el tejido tumoral han sido reportadas como específicas para antígenos tumorales (menos del 10%). Por lo tanto, la mayoría de las células T intratumorales se denominan células T espectadoras (células T espectadoras). La correlación más fuerte con el número de células T convencionales con TCR productivos se observó en las subpoblaciones de células estromales y leucocitos (detectadas por RNA-seq), que pueden usarse para estimar las subpoblaciones de células T (Figura 2a). En los grupos ICR (clasificación general y CMS), la clonalidad más alta de TCR SEQ inmunes se observó en los grupos ICR-alto y subtipo CMS1/inmune (Figura 2c), con la mayor proporción de tumores ICR-alto. Utilizando el transcriptoma completo (18.270 genes), seis genes ICR (IFNG, STAT1, IRF1, CCL5, GZMA y CXCL10) se encontraban entre los diez genes principales asociados positivamente con la clonalidad del TCR inmunoSEQ (Figura 2d). La clonalidad del TCR ImmunoSEQ se correlacionó más fuertemente con la mayoría de los genes ICR que las correlaciones observadas utilizando marcadores CD8+ con respuesta tumoral (Figuras 2f y 2g). En conclusión, el análisis anterior sugiere que la firma ICR captura la presencia de células T amplificadas clonalmente y enriquecidas en tumores, y podría explicar sus implicaciones pronósticas.
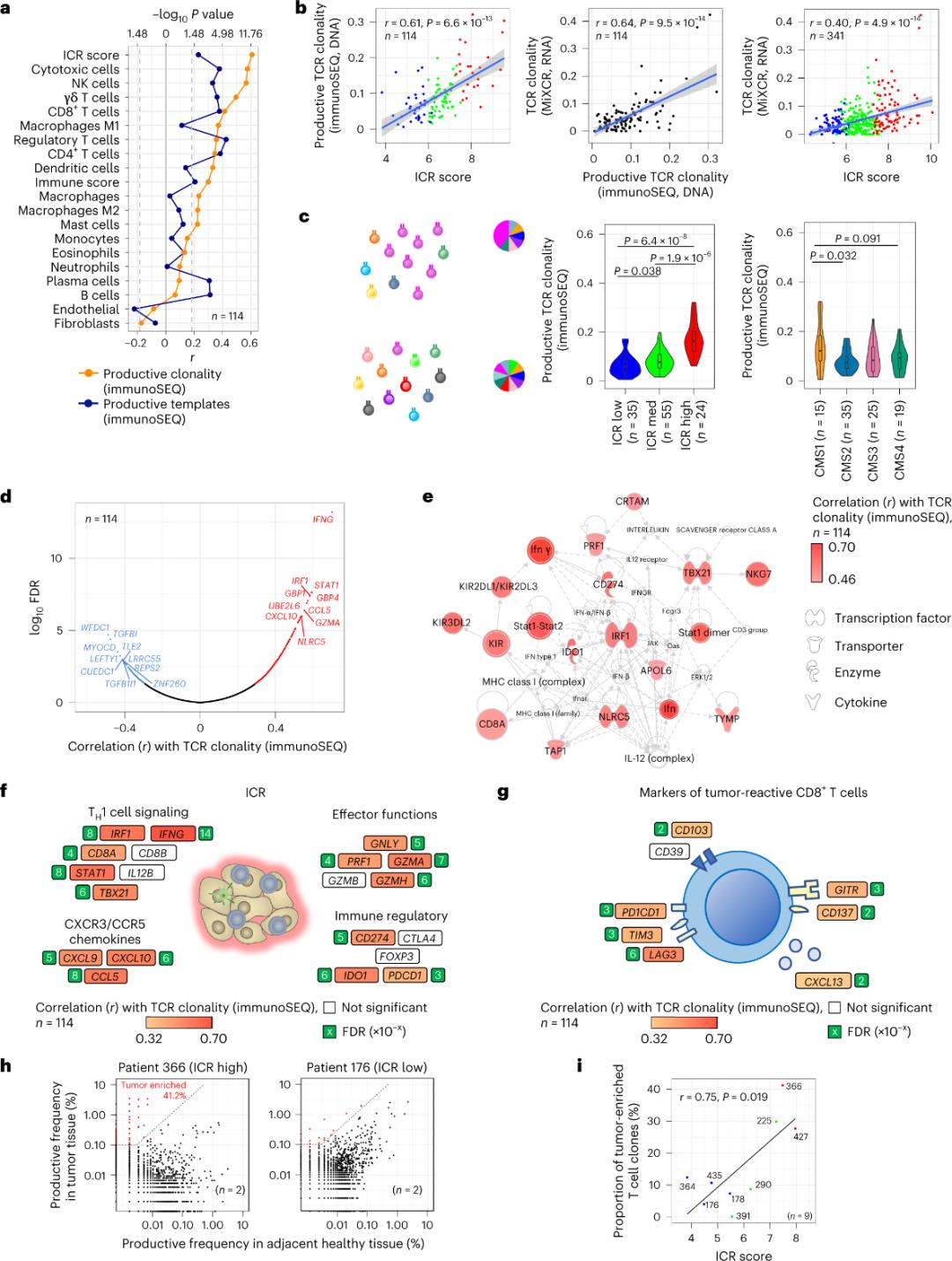
Figura 2. Métricas del TCR y su correlación con genes relacionados con el sistema inmunitario, subtipos inmunitarios y moleculares.
Composición del microbioma en tejidos sanos y de cáncer de colon
Los investigadores realizaron la secuenciación del ARNr 16S utilizando ADN extraído de tejido tumoral y sano de colon de 246 pacientes (Figura 3a). Para la validación, los investigadores analizaron adicionalmente datos de secuenciación del gen del ARNr 16S de 42 muestras tumorales adicionales que no tenían ADN normal correspondiente disponible para el análisis. Primero, los investigadores compararon la abundancia relativa de la flora entre tumores y tejido sano de colon. Clostridium perfringens aumentó significativamente en los tumores en comparación con las muestras sanas (Figura 3a-3d). No hubo diferencia significativa en la diversidad alfa (diversidad y abundancia de especies en una sola muestra) entre las muestras tumorales y sanas, y se observó una modesta reducción en la diversidad microbiana en tumores con ICR alto en relación con tumores con ICR bajo.
Para detectar asociaciones clínicamente relevantes entre los perfiles microbianos y los resultados clínicos, los investigadores se propusieron utilizar datos de secuenciación del gen ARNr 16S para identificar características del microbioma que predigan la supervivencia. En AC-ICAM246, los investigadores ejecutaron un modelo de regresión de Cox OS que seleccionó 41 características con coeficientes distintos de cero (asociadas con un riesgo de mortalidad diferencial), denominadas clasificadores MBR (Figura 3f).
En esta cohorte de entrenamiento (ICAM246), una puntuación MBR baja (MBR<0, MBR baja) se asoció con un riesgo de muerte significativamente menor (85%). Los investigadores confirmaron la asociación entre MBR baja (riesgo) y SG prolongada en dos cohortes validadas de forma independiente (ICAM42 y TCGA-COAD). (Figura 3) El estudio mostró una fuerte correlación entre los cocos endogástricos y las puntuaciones MBR, que fueron similares en el tejido tumoral y el tejido sano del colon.
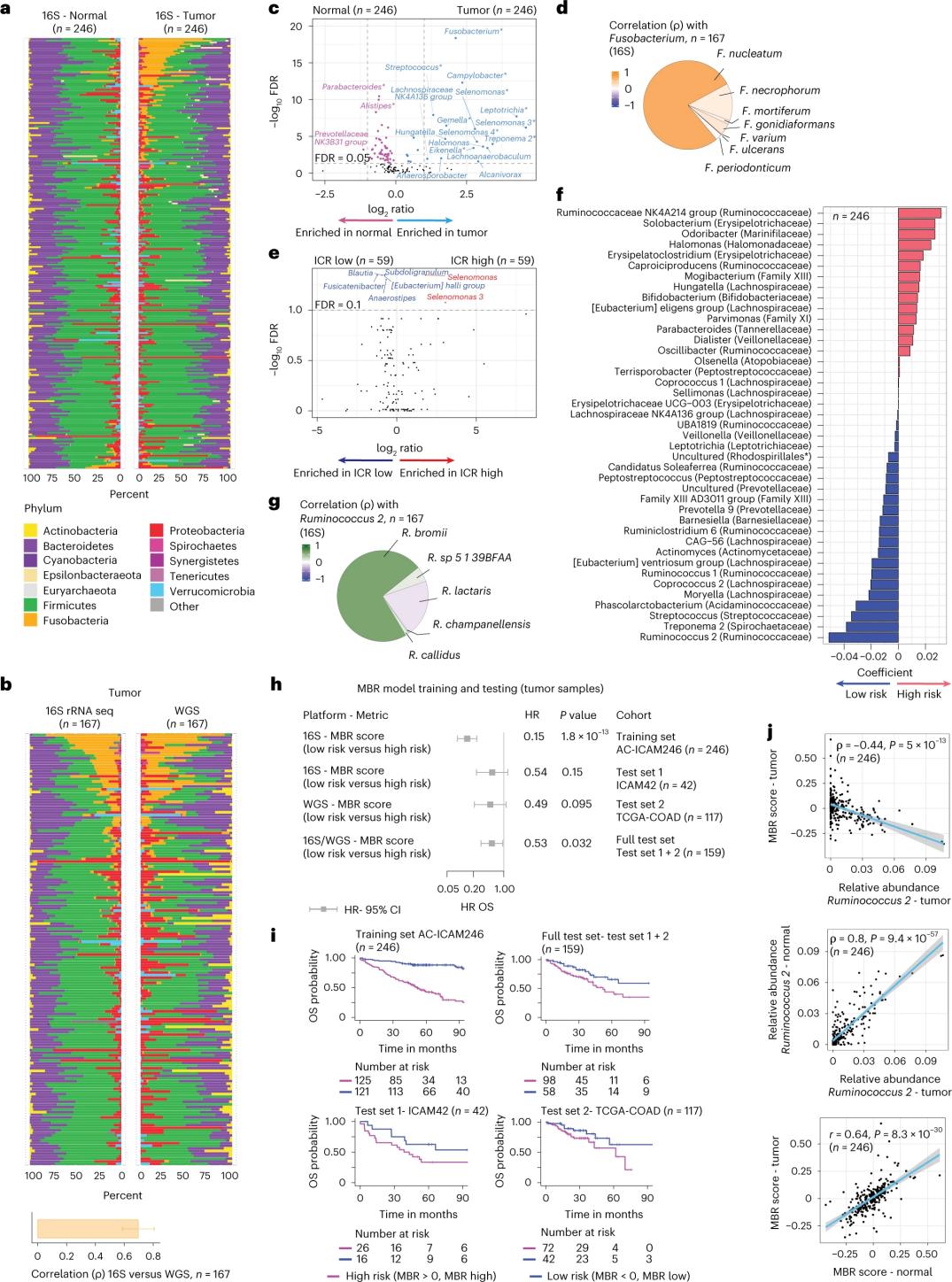
Figura 3. Microbioma en tumores y tejidos sanos y su relación con la ICR y la supervivencia del paciente.
Conclusión
El enfoque multiómico empleado en este estudio permite la detección y el análisis exhaustivos de la firma molecular de la respuesta inmunitaria en el cáncer colorrectal, y revela la interacción entre el microbioma y el sistema inmunitario. La secuenciación profunda del receptor de células T (TCR) en tejidos tumorales y sanos reveló que el efecto pronóstico del ICR podría deberse a su capacidad para capturar clones de células T enriquecidos en el tumor y posiblemente específicos de antígenos tumorales.
Mediante el análisis de la composición del microbioma tumoral utilizando la secuenciación del gen ARNr 16S en muestras AC-ICAM, el equipo identificó una firma microbiana (puntuación de riesgo MBR) con un alto valor pronóstico. Si bien esta firma se derivó de muestras tumorales, se observó una fuerte correlación entre el colon y el recto sanos y la puntuación de riesgo MBR tumoral, lo que sugiere que esta firma podría reflejar la composición del microbioma intestinal de los pacientes. Al combinar las puntuaciones ICR y MBR, fue posible identificar y validar un biomarcador multiómico que predice la supervivencia en pacientes con cáncer de colon. El conjunto de datos multiómicos del estudio proporciona un recurso para comprender mejor la biología del cáncer de colon y contribuir al descubrimiento de enfoques terapéuticos personalizados.
Fecha de publicación: 15 de junio de 2023
 中文网站
中文网站