Durante la reacción de PCR, a menudo se encuentran algunos factores que interfieren.
Debido a la altísima sensibilidad de la PCR, la contaminación se considera uno de los factores más importantes que afectan a los resultados de la PCR y puede producir resultados falsos positivos.
Igualmente importantes son las diversas causas de resultados falsos negativos. Si uno o más componentes esenciales de la mezcla de PCR o de la propia reacción de amplificación se ven inhibidos o interferidos, la prueba diagnóstica puede verse afectada. Esto puede reducir su eficacia e incluso generar resultados falsos negativos.
Además de la inhibición, la pérdida de integridad del ácido nucleico diana puede ocurrir debido a las condiciones de envío o almacenamiento previas a la preparación de la muestra. En particular, las altas temperaturas o un almacenamiento inadecuado pueden dañar las células y los ácidos nucleicos. La fijación de células y tejidos, así como la inclusión en parafina, son causas bien conocidas de fragmentación del ADN y un problema persistente (véanse las figuras 1 y 2). En estos casos, ni siquiera un aislamiento y purificación óptimos serán suficientes.
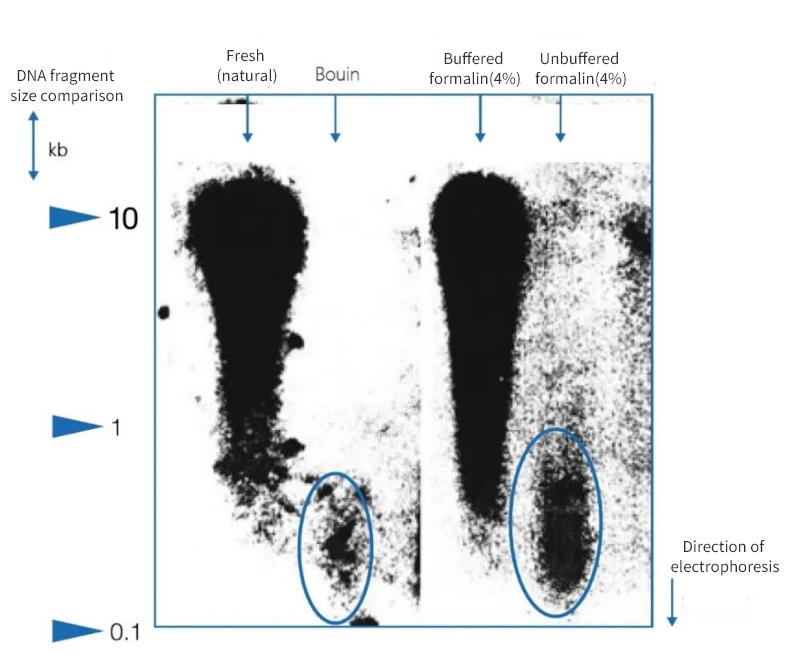
Figura 1 | Efecto de la inmovilización sobre la integridad del ADN
La electroforesis en gel de agarosa reveló que la calidad del ADN aislado de secciones de parafina de autopsias variaba considerablemente. En los extractos se detectó ADN con diferentes longitudes promedio de fragmentos, según el método de fijación. El ADN se conservó únicamente al fijarlo en muestras congeladas nativas y en formalina neutra tamponada. El uso de un fijador de Bouin fuertemente ácido o de formalina sin tamponar con ácido fórmico provocó una pérdida significativa de ADN. La fracción restante se encuentra altamente fragmentada.
A la izquierda, la longitud de los fragmentos se expresa en pares de kilobases (kbp).
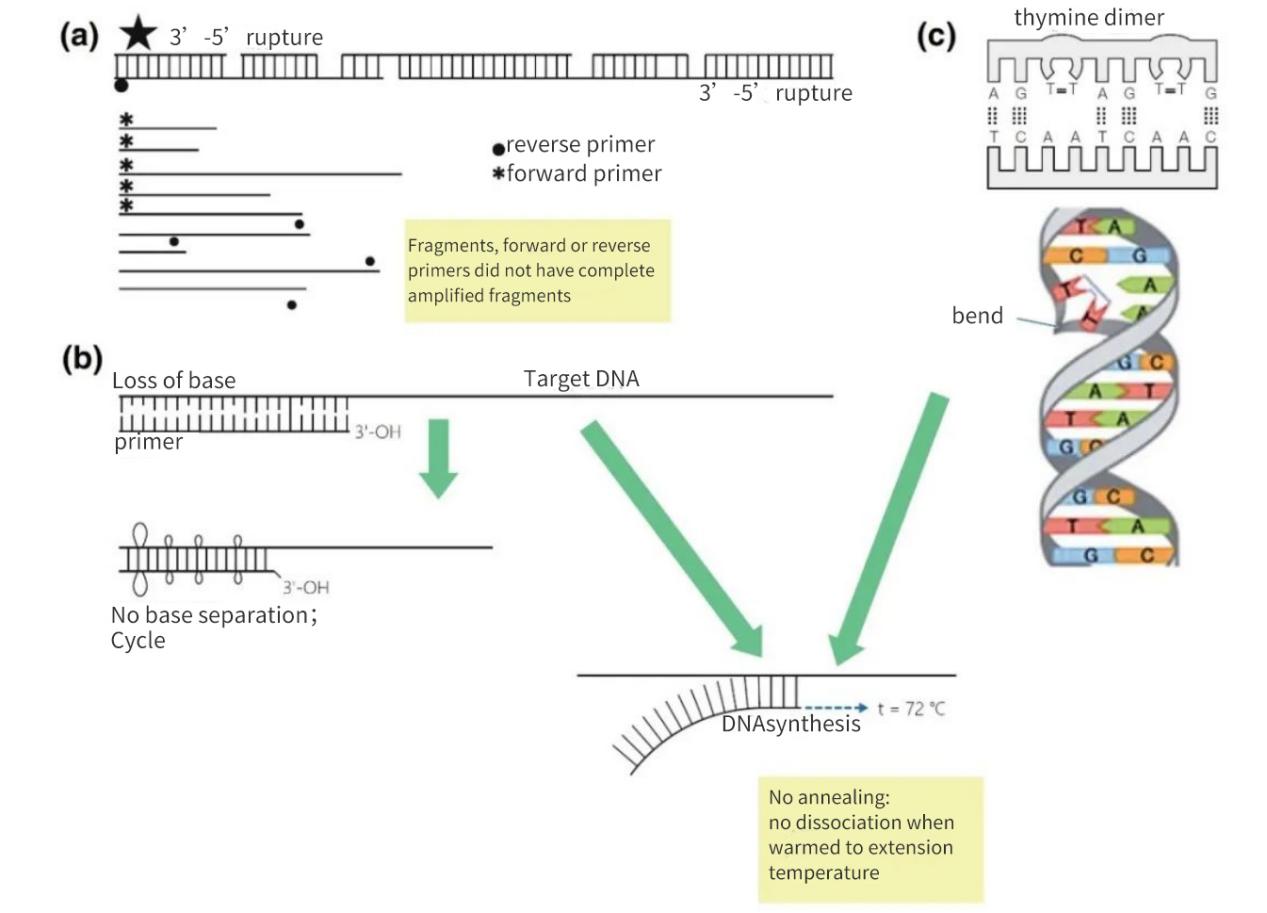
Figura 2 | Pérdida de integridad de los objetivos de ácidos nucleicos
(a) Una brecha 3′-5′ en ambas hebras provocará una ruptura en el ADN diana. La síntesis de ADN continuará en el fragmento pequeño. Sin embargo, si falta un sitio de hibridación del cebador en el fragmento de ADN, solo se producirá una amplificación lineal. En el caso más favorable, los fragmentos pueden re-saturarse entre sí, pero los rendimientos serán bajos y estarán por debajo de los límites de detección.
b) La pérdida de bases, principalmente debido a la despurinación y la formación de dímeros de timidina, conlleva una disminución en el número de enlaces de hidrógeno y una disminución de la Tm. Durante la fase de calentamiento prolongada, los cebadores se separarán del ADN de la matriz y no se hibridarán ni siquiera en condiciones menos rigurosas.
(c) Las bases de timina adyacentes forman un dímero TT.
Otro problema frecuente en el diagnóstico molecular es la liberación subóptima de los ácidos nucleicos diana en comparación con la extracción con fenol-cloroformo. En casos extremos, esto puede dar lugar a falsos negativos. Si bien se puede ahorrar mucho tiempo mediante la lisis por ebullición o la digestión enzimática de los restos celulares, este método suele resultar en una baja sensibilidad de la PCR debido a la liberación insuficiente de ácidos nucleicos.
Inhibición de la actividad de la polimerasa durante la amplificación.
En general, la inhibición se utiliza como concepto general para describir todos los factores que conducen a resultados subóptimos en la PCR. En un sentido estrictamente bioquímico, la inhibición se limita a la actividad de la enzima; es decir, reduce o impide la conversión de sustrato a producto mediante la interacción con el sitio activo de la ADN polimerasa o su cofactor (por ejemplo, Mg2+ para la ADN polimerasa Taq).
Los componentes de la muestra o de los distintos tampones y extractos que contienen reactivos pueden inhibir directamente la enzima o atrapar sus cofactores (por ejemplo, EDTA), inactivando así la polimerasa y, a su vez, provocando una disminución o resultados falsos negativos en la PCR.
Sin embargo, muchas interacciones entre los componentes de la reacción y los ácidos nucleicos que contienen el objetivo también se denominan «inhibidores de la PCR». Una vez que la integridad de la célula se ve alterada por el aislamiento y el ácido nucleico se libera, pueden producirse interacciones entre la muestra y la solución y la fase sólida circundantes. Por ejemplo, los «secuestradores» pueden unirse al ADN de cadena simple o doble mediante interacciones no covalentes e interferir con el aislamiento y la purificación al reducir la cantidad de objetivos que finalmente llegan al recipiente de reacción de la PCR.
En general, los inhibidores de la PCR están presentes en la mayoría de los fluidos corporales y reactivos utilizados para pruebas de diagnóstico clínico (urea en la orina, hemoglobina y heparina en la sangre), suplementos dietéticos (componentes orgánicos, glucógeno, grasa, iones Ca2+) y componentes del medio ambiente (fenoles, metales pesados).
| Inhibidores | Fuente |
| iones de calcio | Leche, tejido óseo |
| Colágeno | Tejido |
| Sales biliares | Heces |
| Hemoglobina | En la sangre |
| Hemoglobina | muestras de sangre |
| Ácido húmico | Suelo, planta |
| Sangre | Sangre |
| Lactoferrina | Sangre |
| melanina (europea) | Piel, cabello |
| Mioglobina | Tejido muscular |
| Polisacáridos | Planta, heces |
| Proteasa | Leche |
| Urea | Orina |
| Mucopolisacárido | Cartílago, membranas mucosas |
| Lignina, celulosa | Plantas |
Los inhibidores de la PCR más comunes se encuentran en bacterias y células eucariotas, ADN no diana, macromoléculas de unión al ADN presentes en matrices tisulares y equipos de laboratorio como guantes y plásticos. La purificación de los ácidos nucleicos durante o después de la extracción es el método preferido para eliminar los inhibidores de la PCR.
Actualmente, diversos equipos de extracción automatizados pueden reemplazar muchos protocolos manuales, pero aún no se ha logrado la recuperación y/o purificación completa de los objetivos. Es posible que aún existan inhibidores potenciales en los ácidos nucleicos purificados o que ya hayan ejercido su efecto. Existen diferentes estrategias para reducir el impacto de los inhibidores. La elección de la polimerasa adecuada puede influir significativamente en la actividad de los inhibidores. Otros métodos probados para reducir la inhibición de la PCR son aumentar la concentración de polimerasa o aplicar aditivos como la BSA.
La inhibición de las reacciones de PCR puede demostrarse mediante el uso del control interno de calidad del proceso (IPC).
Es fundamental eliminar mediante un lavado exhaustivo todos los reactivos y soluciones del kit de extracción, como etanol, EDTA, CETAB, LiCl, GuSCN, SDS, isopropanol y fenol, del aislado de ácido nucleico. Dependiendo de su concentración, pueden activar o inhibir la PCR.
Hora de publicación: 19 de mayo de 2023
 中文网站
中文网站